Cho hỗn hợp A gồm \(Al, Zn, Mg\). Đem oxi hoá hoàn toàn 28,6 g A bằng oxi dư thu được 44,6 g hỗn hợp oxit B. Hoà tan hết B trong dung dịch \(H_2SO_4\) thu được dung dịch D. Tính khối lượng muối khan thu được khi cô cạn dung dịch D.

Những câu hỏi liên quan
Oxi hóa hoàn toàn 28,6 gam hỗn hợp X gồm Al, Zn, Mg bằng oxi hóa dư thu được 44,6 gam hỗn hợp oxit Y. Hòa tan hết Y trong dung dịch HCl thu được dung dịch Z. Cô cạn dung dịch Z được hỗn hợp muối khan là
A. 49,8 gam.
B. 100,8 gam.
C. 74,7 gam.
D. 99,6 gam.
Oxi hóa hoàn toàn 28,6 gam hỗn hợp X gồm Al , Zn và Mg bằng oxi dư , thu được 44,6 gam hỗn hợp oxit Y. Hòa tan hoàn toàn Y bằng lượng vừa đủ dung dịch HCl 1M , thu được dung dịch Z. Cô cạn Z , thu được m gam muối khan . Tính giá trị của V và m.
Bảo toàn khối lượng :
\(m_{O_2}=44.6-28.6=16\left(g\right)\)
\(n_{O_2}=\dfrac{16}{32}=0.5\left(mol\right)\)
Bảo toàn O :
\(n_{H_2O}=2n_{O_2}=2\cdot0.5=1\left(mol\right)\)
Bảo toàn H :
\(n_{HCl}=2\cdot n_{H_2O}=2\cdot1=2\left(mol\right)\)
\(V_{dd_{HCl}}=\dfrac{2}{1}=2\left(l\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=44.6+2\cdot36.5-1\cdot18=99.6\left(g\right)\)
Đúng 3
Bình luận (0)
\(n_O=\dfrac{44,6-28,6}{16}=1\left(mol\right)\)
\(n_{HCl}=n_{Cl^-}=n_O=2\left(mol\right)\)
\(m_{muối}=m_{KL}+m_{Cl^-}=28,6+2.35,5=99,6\left(g\right)\)
\(V_{HCl}=\dfrac{2}{1}=2\left(l\right)\)
Đúng 2
Bình luận (0)
Đốt cháy 28,6 gam hỗn hợp gồm Al, Zn, Mg thu được 44,6 gam hỗn hợp oxit. Hòa tan hết oxit trong dung dịch HCl thu được dung dịch D. Cô cạn dung dịch D thu m gam chất muối khan là
A. 99,6 gam
B. 74,7 gam
C. 49,8 gam
D. 100,8 gam
Trong oxit, mO=44,6-28,6=16 gam =>nO=1 mol
Bảo toàn điện tích trong muối =1.2=2 mol
=>m Muối=28,6+2.35,5=99,6 gam
Đáp án là A
Đúng 0
Bình luận (0)
Đốt cháy 28,6 gam hỗn hợp gồm Al, Zn, Mg thu được 44,6 gam hỗn hợp oxit. Hòa tan hết oxit trong dung dịch HCl thu được dung dịch D. Cô cạn dung dịch D thu m gam chất muối khan là A. 99,6 gam B. 74,7 gam C. 49,8 gam D. 100,8 gam
Đọc tiếp
Đốt cháy 28,6 gam hỗn hợp gồm Al, Zn, Mg thu được 44,6 gam hỗn hợp oxit. Hòa tan hết oxit trong dung dịch HCl thu được dung dịch D. Cô cạn dung dịch D thu m gam chất muối khan là
A. 99,6 gam
B. 74,7 gam
C. 49,8 gam
D. 100,8 gam
Oxi hóa 26,8g hỗn hợp Al,Zn,Fe, bằng oxi thu được 44,6 g hỗn hợp rắn B( chỉ toàn oxit) .Hòa tan hỗ hợp B bằng HCl dư thì thu được dung dịch D. tính mmuối thu được khi cô cạn dung dịch D
Cho hỗn hợp A gồm bột của 3 kim loại: Al, Zn, Mg. Cho 28,6g hỗn hợp A tác dụng hết với oxi(dư) được 44,6g hỗn hợp oxit B. Hòa tan hoàn toàn hỗn hợp B trong dung dịch HCl(dư) được dung dịch D. Cô cạn dung dịch D thu được bao nhiêu g muối khan?
đặt số mol Al, Zn, Mg lần lượt là a, b, c
2Al + 3O2 ---> Al2O3 (1)
Zn + O2 ----> ZnO (2)
Mg + O2 ---> MgO (3)
Al2O3 + 6HCl ---> AlCl3 + 3H2O (4)
ZnO + 2HCl ---> ZnCl2 + H2O (5)
Mg + 2HCl ---> MgCl2 + H2O (6)
dung dịch D thu được là AlCl3, ZnCl2, MgCl2 và HCl dư
cô cạn dung dịch thu được chất rắn là AlCl3, ZnCl2, MgCl2 (HCl bay hơi hết)
hhA ---> hh oxit B
nên => mO trong hhB = mB -mA = 44,6 -28,6 = 16 gam
theo pư (1,2,3) nO trong hỗm hợp B = 16:16 = 1mol
ta lại thấy nO trong nước của pư (4,5,6) = nO trong B = 1 mol
theo pư (4,5,6) nCl trong HCl = 1/2nO trong H2O = 0,5 mol
=> mD = mA + mCl = 28,6 + 35,5*0,5 = 46,35 gam
Đúng 0
Bình luận (0)
Cho hh A gồm Zn, Al, Fe đem oxi hoá 28,6(g) A bằng oxi, thu đc 44,6(g) hh rắn B chỉ gồm các oxit. Hoà tan hết B trong dd HCl thu đc dd D. Khô cạn dd D thu đc hh muối khan có khối lượng là bao nhiêu ?
Mki đang cần gấp mn giúp mk vs ạ, cảm ơn ạ.
\(m_{O_2}=44.6-28.6=16\left(g\right)\)
\(n_{O_2}=\dfrac{16}{32}=0.5\left(mol\right)\)
\(n_{HCl}=2n_{H_2O}=4n_{O_2}=0.5\cdot4=2\left(mol\right)\)
\(m_{Muối}=m_{Kl}+m_{Cl-}=28.6+2\cdot35.5=99.6\left(g\right)\)
Đúng 1
Bình luận (1)
Oxi hóa 26,8g hỗn hợp Al,Zn,Fe bằng õi thu được 44,6 g hỗn hợp rắn B ( chỏ toàn oxit) hòa tan hỗn hợp B bằng dung dịch HCl dư thì thu được dung dịch D . Tính mmuối thu được khi cô cạn dung dịch D
Bạn sửa đề giúp mình.
Cho hỗn hợp A gồm Al, Zn, Mg. Đem oxit hóa hoàn toàn 28,6 gam A bằng oxi dư thu được 44,6 gam hỗn hợp oxit B. Hòa tan hết B trong dung dịch HCl thu được dung dịch D. Cô cạn dung dịch D được hỗn hợp muối khan là?
Giải :
Tham KhảoGọi M là kim loại đại diện cho ba kim loại trên với hóa trị là n.
M + ![]() O2
O2 ![]() M2On (1)
M2On (1)
M2On + 2nHCl ![]() 2MCln + nH2O (2)
2MCln + nH2O (2)
Theo phương trình (1) và (2) ![]() nHCl = 4.
nHCl = 4.![]()
Áp dụng bảo toàn khối lượng ![]()
![]() = 44,6 - 28,6 = 16 (gam)
= 44,6 - 28,6 = 16 (gam)
![]()
![]() = 0,5 mol
= 0,5 mol ![]() nHCl = 4.0,5 = 2 (mol)
nHCl = 4.0,5 = 2 (mol) 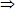 nCl- = 2 mol.
nCl- = 2 mol.
mmuối = mhh kim loại + mCl- = 28,6 + 2.35,5 = 99,6 (gam).
Đúng 0
Bình luận (0)
Cho hh A gồm bột của 3 KL: Al, Zn, Mg. Cho 28,6 g hh A tác dụng hết với oxygen (dư) được 44,6 g hỗn hợp oxide B. Hòa tan hoàn toàn hh B trong dd HCl (dư) được dd D. Cô cạn dd D thu được bao nhiêu g muối khan?
\(2\left[H\right]+\left[O\right]->H_2O\\ n_{Cl}=n_H=2n_O=\dfrac{44,6-28,6}{16}.2=2mol\\ m_{muoi}=28,6+35,5.2=99,6g\)
Đúng 3
Bình luận (0)

















